Água Como Substância
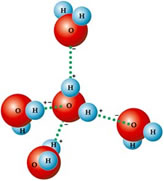
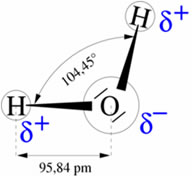
A molécula da água é formada por dois átomos de hidrogęnio ligados a um átomo de oxigęnio por meio de ligaçőes covalentes (figura 1). O ângulo de ligaçăo é de 104,45ş em funçăo da estrutura tetraédrica dos orbitais sp3 do oxigęnio (figura 2).
A água possui, portanto, uma dipolaridade bastante forte com as cargas positivas do hidrogęnio e negativas do oxigęnio, resultando em uma forte rede de ligaçőes intermoleculares. Essas ligaçőes săo denominadas "pontes de hidrogęnio" e săo interagidas pela "força de Van der Waals".
As propriedades da água săo determinadas pelo ângulo de ligaçăo. Se a água apresentasse um ângulo de 180ş entre as ligaçőes, talvez ela năo fosse um líquido ŕ temperatura ambiente.
PROPRIEDADES DA ÁGUA - ESTADO FÍSICO
Sólido
A água apresenta menor densidade no estado sólido do que no estado líquido, o que explica por que o gelo boia sobre a água líquida.
| Temperatura (°C) | Densidade (g/cmł) |
| 100 | 0,9584 |
| 80 | 0,9718 |
| 60 | 0,9832 |
| 40 | 0,9922 |
| 30 | 0,9956502 |
| 25 | 0,9970479 |
| 22 | 0,9977735 |
| 20 | 0,9982071 |
| 15 | 0,9991026 |
| 10 | 0,9997026 |
| 4 | 0,9999720 |
| 0 | 0,9998395 |
| −10 | 0,998117 |
| −20 | 0,993547 |
| −30 | 0,983854 |
Densidade da água em gramas por centímetro cúbico em várias temperaturas em graus Celsius. | |
Geralmente, a água se expande ao congelar devido ŕ sua estrutura molecular aliada ŕ elasticidade incomum das ligaçőes de hidrogęnio e ŕ conformaçăo cristalina particular de baixa energia que ela assume em condiçőes normais de pressăo. Isto é, ao resfriar-se a água tenta organizar-se numa configuraçăo de rede cristalina que alonga as componentes rotacionais e vibracionais das ligaçőes, de forma que cada molécula de água é afastada das vizinhas. Isso efetivamente reduz a densidade p da água quando se forma gelo sob condiçőes normais de pressăo.
Líquido
A água é primariamente um líquido em condiçőes ambientes, o que năo se poderia prever, uma vez que os outros hidretos análogos da família do oxigęnio da tabela periódica săo gases como o sulfeto de hidrogęnio, por exemplo. A razăo pela qual o hidreto de oxigęnio (água) forma um líquido está baseada no fato de ele ser mais eletronegativo que todos esses elementos (exceto pelo flúor).
O oxigęnio atrai elétrons muito mais fortemente que o hidrogęnio, levando a uma carga resultante positiva nos átomos de hidrogęnio e a uma carga resultante negativa no átomo de oxigęnio. A presença de carga nesses átomos dá ŕ água um "momento dipolo". A atraçăo elétrica devida a esse dipolo aproxima as moléculas de água, tornando mais difícil separá-las e, por consequęncia, elevando o ponto de ebuliçăo.
A água pode ser vista como um líquido polar que se dissocia minimamente num íon hidrônio (H3O+ aq) e num íon hidroxila (OH- aq) associado. A água está em equilíbrio dinâmico entre os estados líquido, sólido e gasoso nas condiçőes ambientes de temperatura e pressăo e é a única substância pura encontrada naturalmente na Terra com essa característica.
Gasoso
As pontes de hidrogęnio também săo responsáveis por esta característica. Para evaporar a água, primeiro deve-se romper as pontes de hidrogęnio e, posteriormente, dotar as moléculas de água de suficiente energia cinética para se passar para a fase gasosa. Para evaporar 1 grama de água precisa-se de 540 calorias a uma temperatura de 20şC.
Como o gás, o vapor d'água é completamente miscível com o ar. Por outro lado, a pressăo máxima de vapor termodinamicamente estável com a líquida (ou sólida) numa dada temperatura é relativamente baixa se comparada com a pressăo atmosférica total. Por exemplo, se a pressăo parcial de vapor for 2% da pressăo atmosférica e o ar for resfriado a partir de 25şC, aos cerca de 22şC a água começa a condensar-se, definindo o ponto de orvalho, formando neblina ou orvalho.
O processo inverso faz com que a neblina "desapareça" pela manhă. Se a umidade aumenta ŕ temperatura ambiente (por exemplo, devido a um chuveiro quente) e a temperatura se mantém a mesma, a água gasosa logo chega ŕ pressăo de mudança de fase e se condensa como vapor. Um gás nesse contexto é dito saturado ou a 100% de umidade relativa quando a pressăo e o vapor d'água no ar estăo em equilíbrio com a pressăo de vapor devido ŕ água (líquida).
Autores
Lauro de Oliveira Silva Júnior
Lúcio Carramillo Caetano
Fontes
Wikipedia, acessado em 07/01/2010.
Macedo Barros Águas & Águas, 2004.





